闫金松医生的科普号
- 精选 什么是输血依赖的重型再生障碍性贫血?
大连医科大学附属第二医院血液科 闫金松1什么是输血依赖的重型再生障碍性贫血?输血依赖的重型再生障碍性贫血,我们将其定义为重型再生障碍性贫血-II型(SAA-II),其临床特点如下:1) 病人在初次发病时表现为非重型再生障碍性贫血,2) 但随着疾病的进展,患者贫血逐步加重,并达到重型再生障碍贫血的诊断标准;中性粒细胞缺乏,严重贫血,血小板非常低下;3) 在疾病的进展过程中,长期口服环孢素等免疫抑制剂、雄激素、糖皮质激素、甚至多种中药,但均反应不佳;4) 病程中反复感染、频繁使用抗生素导致多种抗生素耐药;5) 反复输血、输注血小板导致红细胞及血小板的输注无效;6) 血清铁蛋白显著升高;7) ATG治疗无效;8) 发病至移植的中位病程长达8年(1-22年)以上;9) 只能采取异基因骨髓移植的治疗方法。2、输血依赖的重型再生障碍性贫血的2个病例1) 病例1:12岁的小田,9岁时出现血细胞的显著减少,就诊于当地医院,反复输血支持,后因周身无力、出血、感染等无法正常上学,首先筛查是否存在先天遗传病导致的骨髓衰竭,之后在明确除外了范可尼贫血、Wiskott-Aldrichsyndrome(WAS)等遗传病,最终确诊“慢性再障”。就诊时病情已加重,一年内无数次输血及血小板才能艰难活着,走路走不动,生活不能自理,考虑存在输血依赖,为一类输血依赖的重型再生障碍性贫血,我们将其定义为“重型再障II型”。2) 病例2:7岁的小马,呀呀学语时就不幸确诊为“慢性再障”,辗转于多家医院就医,长期口服环孢素、达那唑、中医偏方等药物治疗,效果不理想,乏力、出血等症状进行性加重,同样经历4年多的相关治疗,病情持续加重,输血依赖,最终进展为“重型再障II型”,反复的输血、输血小板,让他不得放弃上学,在家治疗。针对这样的患儿,究竟该如何治疗才能让他们重获新生呢?3异基因造血干细胞移植可以用于治疗输血依赖的重型再生障碍性贫血上述两位患儿,均采用Flu/Bu/Cy-ATG作为一致的预处理方案,采用其父母的造血干细胞成功重建其造血系统,完成了单倍体造血干细胞移植的治疗。到目前为止,小田已顺利考上了初中,恢复了正常的学习生活。而小马也完成了小学学习,正在选择自己喜欢的初中学校,父母的脸上都洋溢着生活的幸福。骨髓移植治疗输血依赖的重型再障,临床治疗效果显著,因此尽早选择异基因骨髓移植,是治愈该病的治疗方法之一。
闫金松 主任医师 大连医科大学附属第二医院 血液科13人已读 - 精选 BTK 抑制剂可以用于套细胞淋巴瘤吗?
大连医科大学附属第二医院 血液科 闫金松MantleCellLymphoma(MCL)是一种B细胞非霍奇金淋巴瘤,其发生机制主要是:1)t(11;14)(q13;q32)染色体易位,导致cyclinD1基因(CCND1)与IgH基因区域的融合,从而使cyclinD1基因过度表达。CyclinD1是细胞周期调控蛋白,其过度表达促进了细胞增殖并在MCL的发病中起到关键作用。2)B细胞受体信号通路异常:MCL患者的B细胞受体信号通路异常活化,包括B细胞受体和NF-κB信号通路的活化。这种异常信号通路的活化可以促进MCL细胞的生存、增殖和转移。因此,对MCL发生机制的深入理解有助于为该病的治疗提供更有效的靶向治疗策略。 套细胞淋巴瘤患者的B细胞通常存在B细胞受体信号通路的异常活化,BTK是一种关键的信号传导蛋白,在B细胞受体信号通路中发挥重要作用。BTK抑制剂可以通过阻断这一信号通路的活化来抑制淋巴瘤细胞的生长和增殖,因此,BTK(Bruton'styrosinekinase)抑制剂可以用于治疗套细胞淋巴瘤。目前,伊布替尼是一种常用的BTK抑制剂,已经被批准用于一线治疗复发/难治性MCL,在MCL的治疗中具有良好的疗效。它可以单独应用,也可以与其他药物(如Rituximab)联合应用,以提高治疗效果。
闫金松 主任医师 大连医科大学附属第二医院 血液科1人已读 - 精选 套细胞淋巴瘤与自体造血干细胞移植
大连医科大学附属第二医院血液科闫金松对于套细胞淋巴瘤MCL患者,自体造血干细胞移植是一种治疗选择,尤其是对于年轻且符合条件的患者。ASCT可以在化疗后达到完全缓解,首先通过高剂量的化疗药物杀灭MCL细胞,通过自体造血干细胞移植可以重建患者的造血系统。ASCT包括如下程序:1)采集干细胞:完全缓解的患者通过骨髓或外周血采集足够数量的造血干细胞,然后冷冻保存造血干细胞。2)高剂量化疗清除体内淋巴瘤残留:采集干细胞后,患者接受高剂量的化疗,以尽可能的清除体内的MCL淋巴瘤细胞。3)干细胞移植:在预处理化疗后,患者接受造血干细胞回输。回输的造血干细胞注入患者的体内后,随后进入并定植在骨髓,之后重建造血功能。4)植入及恢复期:患者在移植后会经历一个造血重建,之后进入恢复期,这段时间内患者的免疫系统和造血功能都会逐渐恢复。自体造血干细胞移植对于MCL的治疗可以通过高剂量的化疗及预处理化疗,尽可能清除患者体内的MCL细胞,通过回输造血干细胞,重建免疫和造血后,有望显著提高MCL淋巴瘤患者的临床治愈率。
闫金松 主任医师 大连医科大学附属第二医院 血液科暂无已读 - 精选 套细胞淋巴瘤简介
大连医科大学附属第二医院血液科闫金松套细胞淋巴瘤(Mantlecelllymphoma,MCL)是一种非霍奇金淋巴瘤的亚型,通常被认为是一种侵袭性的淋巴瘤,通常累及淋巴结、脾脏、骨髓等。MCL的发病机制涉及基因突变、染色体异常和信号通路的失调。其中,t(11;14)染色体易位是MCL最特征性的遗传异常,导致cyclinD1基因(CCND1)的过度表达,促进细胞周期的进程,从而促进MCL淋巴瘤的发展。MCL通常被分为两种亚型:经典型MCL和MCL变异亚型。经典型MCL是最常见的亚型,通常表现为淋巴结肿大、脾脏肿大、外周血液中的淋巴细胞增多等症状。MCL变异亚型则表现出较低的淋巴结受累程度,但可能具有更具侵袭性的特点。治疗MCL的方法通常包括化疗、靶向治疗、自体干细胞移植等。虽然MCL在临床上被认为是一种难治性的淋巴瘤,但近年来的治疗进展已经提高了患者的预后和生存率。
闫金松 主任医师 大连医科大学附属第二医院 血液科1人已读 - 精选 移植物抗宿主病(GVHD)
大连医科大学附属第二医院血液科 闫金松骨髓移植后的并发症之一是GVHD,是由供者细胞与患者组织发生反应导致的临床综合征,分为急性和慢性GvHD。经典急性GvHD发生在移植后100天内,主要表现为皮肤、胃肠道和肝脏三个器官的炎症反应。一、GVHD的分度:按严重程度可将急性GvHD分成I-IV度,发生率50%-60%,III-IV度以上急性GvHD发生率15%左右,死亡率高达50%。其中下消化道急性GVHD以水样腹泻表现为主,重度肠道GvHD(III-IV级)表现为腹痛、便血和肠梗阻,下消化道急性GVHD与移植后非复发相关死亡密切相关。二、治疗原则1)激素在急性GVHD的治疗中仍然是一线推荐药物,最新的研究进展为新药与激素联合使用的策略,即激素加新药方案,以提高GVHD的治疗效果和反应率,并同时确保激素的逐渐减量。2)激素加新药方案包括激素与芦可替尼、巴利昔单抗、环磷酰胺、、西罗莫司及间充质干细胞等新药物联合使用。这种新的尝试可能会为激素的一线治疗带来更多患者的受益和病情的稳定控制。
闫金松 主任医师 大连医科大学附属第二医院 血液科62人已读 - 精选 儿童重型再生障碍性贫血免疫治疗现状
大连医科大学附属第二医院血液科闫金松目前国际上针对重型再障的治疗主要分为三大类,一线治疗主要采用免疫抑制治疗,比如口服环孢素及输注红细胞、血小板等对症治疗,不能治愈疾病,仅仅控制其发展,67%的患儿最终仍会发生疾病进展,总体治疗有效率约为60%,且仅采用支持治疗的患儿死亡率高达80%。其次,还可应用抗胸腺细胞球蛋白(ATG)进行联合免疫治疗,治疗5年有效率达60-70%,不良反应相对少见,适用于无法进行移植的患者。但其中约30-40%患儿治疗无效或复发,仍未能脱离感染、出血风险及血制品输注依赖等并发症。最根本的治愈方法就是异基因造血干细胞移植,尤其是单倍体造血干细胞移植,现已确立为SAA最主要的治疗手段。目前3年治疗有效率达87-92%,适用于年龄小于40岁,存在HLA半合供者或者免疫抑制治疗失败的患者,但需注意移植后急慢性移植物抗宿主病的发生,一般发生率为30%,及时调整用药一般可有效控制。但是,对于输血依赖的重型再生障碍性贫血,上述免疫治疗的方法疗效不确定,异基因造血干细胞移植是目前可以选择的治疗手段。
闫金松 主任医师 大连医科大学附属第二医院 血液科23人已读 - 精选 二次单倍体造血干细胞移植治疗重型再生障碍性贫血移植失败患者
大连医科大学附属第二医院血液科 闫金松大连医科大学附属第二医院血液科闫金松教授移植团队,应用含ATG预处理方案的单倍体移植治疗8例移植失败的SAA患者,中位随访时间61个月(5年),6例患者存活,5年总体生存率75%[8],证实含ATG预处理方案的单倍体移植治疗移植失败的重型再生障碍性贫血患者是可行且有效的,该文章发表于ScientifcReports杂志上(IF4.6):ZhangC,HouY,YangY,ZhangJ,ZhengX,YanJ.Secondhaploidenticalbonemarrowtransplantationwithantithymocyteantibody-containingconditioningregimenforgraftfailureineightpatientswithsevereaplasticanemia.SciRep.2024;14(1):2293. 重型再生障碍性贫血(SAA)是一种严重危及患者生命的获得性骨髓造血功能衰竭综合征,异基因造血干细胞移植(allo-HSCT)是SAA患者首选治疗方法,5年总体生存率可高达90%。但是部分患者的植入失败仍是影响接受SAA患者长期生存的重要因素。二次造血干细胞移植是SAA患者移植失败后的唯一治疗手段。含抗胸腺细胞免疫球蛋白(ATG)的单倍体移植方案是挽救首次移植失败SAA患者生命的有效治疗方法。5年总体生存率可达75%。 代表性病例:21岁的小孙是一名大学生,2年前因”鼻衄,发现血小板减少”就诊于大连医科大学附属第二医院血液科,诊断为重型再生障碍性贫血,allo-HSCT为其首选治疗方案,小孙无同胞及非血缘全相合供者,与其父亲行HLA高分辨率配型为5/10相合,选择其父亲作为供者进行单倍体造血干细胞移植,经过预处理后,小孙顺利回输父亲的骨髓和外周血造血干细胞,移植后+14d粒系重建,移植后+20天血小板升高至25×109/L,移植后+25天小孙出现发热,之后中性粒细胞绝对值呈直线下降,移植后+28天降至0,移植后+33骨髓嵌合度降至1.55%,移植失败了。二次造血干细胞移植是小孙唯一的存活希望。小孙接受了二次单倍体造血干细胞移植,因为其母亲患有乙型病毒性肝炎,故继续选择他的父亲作为供者,经过二次预处理后,小孙再次回输了其父亲的骨髓造血干细胞和外周造血干细胞,移植后给予后置环磷酰胺、他克莫司、吗替麦考酚酯预防移植物抗宿主病,经过20多天的等待,二次单倍体移植最终成功。现在小孙二次移植后17个月,已经完全康复,回归正常生活。1.什么是重型再生障碍性贫血?再生障碍性贫血是一种获得性骨髓造血功能衰竭综合征,主要表现为骨髓造血功能低下、全血细胞减少和贫血、出血、感染的综合征。在我国,其年发病率为6~9/百万,高发年龄分别为15~25岁的青壮年和65~69岁的老年人,男、女发病率无明显差异。按疾病严重度分为重型和非重型再生障碍性贫血。重型再生障碍性贫血起病急骤,出血、感染严重,常发生在内脏,内脏感染和败血症,死亡率较高。重型再生障碍性贫血患者的网织红细胞绝对值、中性粒细胞和血小板数明显减低,骨髓增生极度减低,血象需具备下述三项中两项:①网织红细胞绝对值<15×109/L;②中性粒细胞绝对值<0.5×109/L;③血小板<20×109/L。2.异基因造血干细胞移植治疗重型再生障碍性贫血疗效如何?目前治疗SAA的方法主要为allo-HSCT和免疫抑制(IST)治疗(如抗胸腺/淋巴细胞球蛋白联合环孢素A),其中allo-HSCT是最有可能治愈疾病的手段,与IST相比,接受allo-HSCT治疗的患者可以快速重建造血,且一般不需要维持治疗,远期生存率高。根据供者不同,allo-HSCT分为同胞全相合移植、无关供者移植、单倍体移植、脐血移植。同胞全相合移植治疗重型再生障碍性贫血患者,9年的总体生存率仍可达65%~97%。无关供者移植治疗重型再生障碍性贫血患者5年总体生存率达85.7%[3]。单倍体造血干细胞移植治疗儿童重型再生障碍性贫血患者的3年无失败生存率可达91.3%~96.4%。脐带血移植治疗儿童重型再生障碍性贫血患者,3年总体生存率可达84.6%。3.重型再生障碍性贫血患者移植失败后是否还有存活机会?Allo-HSCT治疗SAA的一大障碍是植入失败,发生率为3.8~15%,植入失败后患者会出现严重的骨髓衰竭,并短期内因严重感染、器官衰竭等原因死亡,二次造血干细胞移植是SAA移植失败患者的唯一治疗手段。
闫金松 主任医师 大连医科大学附属第二医院 血液科15人已读 - 精选 自体造血干细胞移植是多发性骨髓瘤的首选治疗
大连医科大学附属第二医院血液科闫金松 自体造血干细胞移植作为多发性骨髓瘤的一线治疗,其治疗地位需要推广。多发性骨髓瘤为克隆性浆细胞异常增殖的恶性疾病,为血液系统第二大恶性肿瘤,现已成为危害人类健康的重大疾病之一,5年的相对总体生存率为54.9%,无病生存时间平均为40个月,总体生存时间平均为54个月。美国国立综合癌症网络(NationalComprehensiveCancerNetwork,NCCN)2023发布的多发性骨髓瘤最新指南中明确指出,即使在新药时代下,对于新发的骨髓瘤患者应及时进行以硼替佐米及地塞米松为基础的三药联合化疗方案,包括联合来那多胺或环磷酰胺,并将此作为一线推荐诱导方案。如患者经过3-4疗程标准化疗后达到部分缓解(partialresponse,PR)以上的缓解深度,一线推荐桥接自体造血干细胞移植术治疗,相较于单纯三药等联合诱导或巩固化疗等方法,可将初诊骨髓瘤患者的无病生存时间延长至48个月,总体生存时间延长至90个月以上,5年总体生存率提高至62%以上,使患者获得长期生存收益1。
 闫金松 主任医师 大连医科大学附属第二医院 血液科18人已读
闫金松 主任医师 大连医科大学附属第二医院 血液科18人已读 - 医学科普 饮食均衡也会得营养性贫血吗?
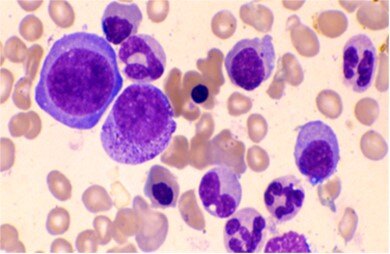
杨岩闫金松(大连医科大学附属第二医院血液科)病例:60岁的张阿姨近半年来时常感到头晕乏力、食欲减退,且症状逐渐加重,近1个月来体重下降明显,甚至出现口腔溃疡、舌痛、手足麻木和上腹胀痛感。为寻求病因,张阿姨就诊于我院血液科门诊,经检查结果显示为大细胞性贫血,血清叶酸、维生素B12均减低,骨髓细胞学提示典型的巨幼样变特征,最终张阿姨被诊断为营养性巨幼细胞性贫血。张阿姨得知诊断结果后很是吃惊,“我平日保养得当、饮食均衡,荤素搭配合理且没有不良饮食习惯,为什么会得这个病呢?”张阿姨百思不得其解。为寻求病因,医生为张阿姨做了更详尽的检查,发现其体内出现了针对壁细胞和内因子的自身抗体,从而激发自身免疫性炎症反应使胃壁细胞总数减少,致使与维生素B12结合的内因子减少、维生素B12吸收不良,最终出现营养性巨幼细胞性贫血。 1什么是营养性巨幼细胞性贫血?营养性巨幼细胞性贫血简称巨幼贫,多由体内缺乏维生素B12和(或)叶酸而造成的脱氧核糖核酸(DNA)合成障碍所引起的一种大细胞贫血。其特点是骨髓内出现巨幼红细胞,粒系、巨核系也可出现巨幼样变。该类巨幼细胞易在骨髓内被破坏,出现无效的红细胞。除造血细胞,维生素B12缺乏时还可出现神经系统症状。2营养性巨幼细胞性贫血的病因有哪些?(一)叶酸缺乏原因:①摄取不足、空肠疾病、药物影响②需求增加:妊娠、早产、慢性溶血、恶性肿瘤、慢性炎性疾病③自身丢失:长期透析、某些皮肤病(二)维生素B12缺乏原因:①摄入不足②食物中维生素B12释放障碍:胃酸不足(胃壁细胞抗体、胃大部切除)、内因子分泌不足、维生素B12-内因子复合物释放障碍、回肠疾病③微生物因素:肠道菌群失调④药物类:双胍类、氨基水杨酸3营养性巨幼细胞性贫血临床表现有哪些?(一)血液系统症状:贫血为中度至重度,除伴有乏力、头晕、活动后心悸和气短外,可有轻度溶血表现,如皮肤、巩膜黄染,可有轻度黄疸和脾脏肿大。 (二)消化系统症状:如食欲不振、恶心、腹泻、腹胀及便秘等,口腔溃疡、舌质红、舌痛、舌乳头萎缩、表面光滑出现牛肉舌。 (三)神经系统症状:维生素B12缺乏可出现神经系统症状,主要为脊髓后侧束变性,表现为手足对称性麻木、深感觉障碍、共济失调、步行障碍,亦可同时出现周围神经病变及精神抑郁。4营养性巨幼细胞性贫血如何诊断?(一)临床表现:①贫血症状②消化道症状③神经症状(二)实验室检查:①大细胞性贫血,MCV>100fL,红细胞呈大卵圆形。②白细胞和血小板亦可减少。中性粒细胞核分叶过多,网织红细胞亦可减低、正常或轻度增高。③骨髓呈典型的巨幼样改变,巨幼细胞>10%,粒细胞系统及巨核细胞系统有巨形变。④生化检查:血清维生素B12测定<74pmol/L(100ng/ml);血清叶酸测定<6.8nmol/L(3ng/ml)。5营养性巨幼细胞性贫血如何治疗?补充叶酸和(或)维生素B12是该病的基本治疗方法。对摄入不足者应调整饮食结构,对吸收障碍或丢失过多者,在外源性补充叶酸和(或)维生素B12同时应治疗相应基础疾病。6营养性巨幼细胞性贫血的预后如何?巨幼细胞性贫血预后较好,给予补充叶酸和(或)维生素B12都可以使临床症状迅速改善,神经系统症状恢复较慢或不恢复,一般在治疗3-12个月后,约90%的神经系统症状可恢复。
 闫金松 主任医师 大连医科大学附属第二医院 血液科46人已读
闫金松 主任医师 大连医科大学附属第二医院 血液科46人已读 - 学术前沿 单倍体骨髓移植治疗重型再生障碍性贫血-II型具有积极乐观的临床效果
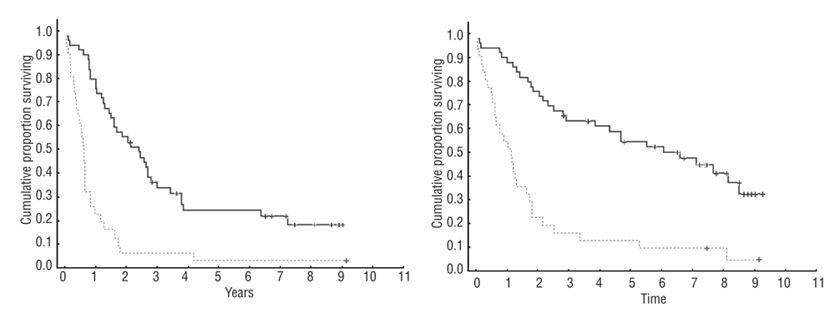
近日,英文期刊Frontiers of Medicine在线发表了大连医科大学附属二院血液科闫金松团队作为第一单位及通讯作者身份撰写的论文 “Outcomes of haploidentical bone marrow transplantation in patients with severe aplastic anemia-II that progressed from non-severe acquired aplastic anemia”(半相合骨髓移植治疗慢性再生障碍性贫血进展的重型再生障碍性贫血-II型的疗效观察)。该文第一作者为该院血液科主治医师刘虹辰,毕业于德国科隆大学,获内科学博士学位,擅长血液疾病的精准诊疗及骨髓移植工作。国际上常将再生障碍性贫血分为重型再生障碍性贫血(SAA)及非重型再生障碍性贫血(NSAA)。SAA 常见于儿童患者,起病急、病情重、治疗难度大、死亡率高,以胸腺淋巴细胞球蛋白(ATG)为主的联合免疫强化治疗,有效率可达到65%以上,但单倍体骨髓移植有效率可以提高至90%以上。本篇文章对重型再生障碍性贫血-II型(SAA-II)进行了定义:值得关注的是,符合重型再生障碍性贫血标准的患者中,存在一个特殊的患者群体,病人在初次发病时表现为NSAA,但随着疾病的进展,患者贫血逐步加重,并达到SAA 的诊断标准,在本研究中,将该类疾病定义为SAA-II(重型再生障碍性贫血-II型)。该类患者呈现不同于初发SAA的临床特点:在疾病的进展过程中,长期口服环孢素等免疫抑制剂、雄激素、糖皮质激素、甚至多种中药,但均反应不佳;病程中反复感染、频繁使用抗生素导致多种抗生素耐药;反复输血、输注血小板导致红细胞及血小板的输注无效;血清铁蛋白显著升高;ATG 治疗无效;发病至移植的中位病程长达8年(1-22年)以上,上述临床特点导致单倍体骨髓移植的治疗风险及难度很大。该文回顾性观察了2015年至2018年,22例接受单倍体移植治疗的再生障碍性贫血-II型(SAA-II)患者,总结分析了SAA-II型患者的临床特征、病程、外周血象特点、供体类型、预处理方案的组成、植入率、急慢性排异反应的发生率、病毒再激活、总体生存时间等指标。鉴于目前该部分患者临床上没有常规的治愈方案,以Flu/Bu/Cy-ATG作为预处理方案的单倍体移植,遵循了“北京方案”的基本原则,22例SAA-II型患者中,21例(95.5%)获得了的稳定植入,仅3例死亡,获得了86.4%的长期生存。共有4例发生II-IV急性排异反应,其中仅2例发生III-IV 排急性排异反应,并均得到良好控制和恢复。需要特别提到的是,其中12例(54.5%)移植过程中发生了细菌和真菌感染,提示SAA-II患者最好在疾病进展至非常严重的阶段之前,尽早开展移植治疗,以减少移植过程中感染发生的风险。总之,该篇回顾性报告发现,单倍体骨髓移植是治疗SAA-II 的良好选择之一,取得了积极乐观的临床治疗效果。对SAA-II患者,在缺少同胞全合供者的情况下,尽早选择单倍体骨髓移植,是一个值得接受的良好的治疗方案,值得采用。
闫金松 主任医师 大连医科大学附属第二医院 血液科881人已读





